石家庄脂质体载药研发
酸性环境(pH值2.0-4.0)通常⽤于产⽣⽤于活***物装载的跨膜pH梯度。在37℃和pH2.0条件下,SM/Chol脂质体(55/45,mol/mol)的⽔解速率⽐DSPC/Chol脂质体慢约100倍。此外,含有SM/Chol的脂质体表现出比较好的药代动⼒学特性,即增加循环时间并增强药物向靶组织的递送。胆固醇(Chol)是脂质体双分⼦层的另⼀个主要成分,⼏乎可以⽤于所有的商业产品。Chol的加⼊可以促进脂链的堆积和双分⼦层的形成,调节膜的流动性/刚性,并进⼀步影响药物释放、脂质体的稳定性和胞外分泌动⼒学。对于Shingrix(带状疱疹疫苗,含有糖蛋⽩E抗原和AS01B脂质体佐剂系统)的产物,Chol可以避免QS21(AS01B佐剂系统中的免疫增强剂之⼀)以2:1的⽐例(Chol:QS21,w/w)⽔解。对于AmBisome的产物,与⾮甾醇相⽐,Chol降低了脂质体制剂的毒性。Chol对双分⼦层性质的影响是浓度依赖性的。据报道,低浓度(2.5mol%)和⾼浓度(>30mol%)的Chol对脂质双分⼦层的性质影响不⼤。5<Cholmol%<30的Chol的“冷凝效应”或“有序效应”导致颗粒⼤⼩从220nm逐渐增⼤到472nm,膜的流动性降低,药物释放减少。除了Chol,其他与Chol结构相似的甾醇,如⻩体酮、⻨⻆甾醇和⽺⽑甾醇,也被研究⽤于调节膜的刚性和稳定性。脂质体表⾯修饰的作用。石家庄脂质体载药研发
脂质体共价连接药物-脂质偶联载***式通过连接剂将药物分⼦与脂质共价连接是另⼀种在脂质体内装载药物的有效策略,例如Mepact。MDP是主要⾰兰⽒阳性菌细胞壁的组成部分,具有****应答的作⽤。由于MDP是⽔溶性低分⼦量分⼦,其脂质体在储存过程中存在包封效率低和药物泄漏等问题。为了提⾼MDP的脂溶性,通过肽间隔剂将MDP与PE连接,合成MTP-PE(muramyltripeptide-phosphatidylethanolamine)。在⽤⽣理盐⽔重建冻⼲产物(MTP-PE,POPC和OOPS)时,MTP-PE的两亲分⼦嵌⼊脂质体的膜双层。脂质体内存在MTP-PE,未发现游离MTP-PE。Vyxeos采⽤被动加载和主动加载相结合的⽅法,这是⾸个被批准在同⼀囊泡中加载两种不同药物(阿糖胞苷和柔红霉素)的脂质体。简⽽⾔之,当脂质泡沫与Cu(葡糖酸盐)2、三⼄醇胺(TEA)、pH7.4和阿糖胞苷溶液⽔合时,阿糖胞苷被被动地封装到脂质体中。经过减浆和缓冲液交换以去除未包封的药物和Cu(葡糖酸盐)2/TEA后,中性pH的柔红霉素缓冲液与载糖胞苷脂质体孵育。江西脂质体载药药物含有DOTAP、胆固醇和DSPC-PEG2000的阳离子脂质体可以递送microRNA 。

siRNA脂质体
RNA干扰(RNAi)途径允许siRNA和miRNAs负向调节蛋白表达。siRNA是21~23对核苷酸组成的双链RNA,可诱导同源靶mRNA沉默。为了发挥作用,双链siRNA分裂成两个单链RNA:乘客链和引导链。乘客链被argonaute-2蛋白降解,而引导链则被纳入RNAi诱导的沉默复合体中,该复合体结合与引导链互补的mRNA并将其切割。siRNA似乎具有***多种疾病的巨大潜力,因为它们可以很容易地下调各种靶mRNA,而不考虑它们的位置(即在细胞核或细胞质中),并且它们的特异性结合表明它们比传统化学药物诱导的副作用更少。作为一种新型的基于核酸的***策略,siRNA***与传统的化学药物相比具有许多优势。然而,为了促进基于siRNA的***方法的发展,必须克服一些挑战,包括需要识别适当的靶基因和开发优化的递送系统。许多研究人员试图利用阳离子脂质体提高siRNA的细胞递送和基因沉默效率。例如,由DC-6-14、DOPE和胆固醇组成的阳离子脂质体被用于递送萤火虫荧光素酶特异性的siRNA。当阳离子脂质体与siRNA持续剧烈搅拌混合时,转染效率提高,说明将siRNA加载到阳离子脂质体上的方法可以调节转染效率。siRNA脂丛的***应用因靶蛋白而异。
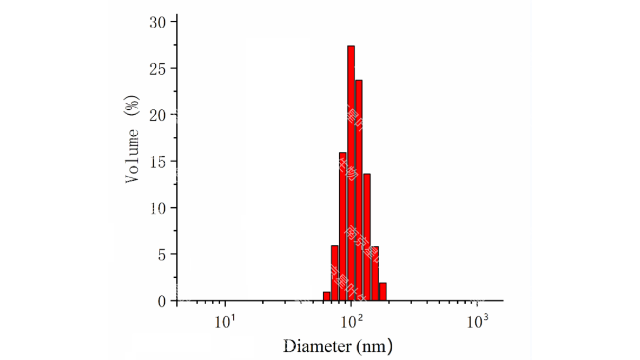
脂质体的粒径和粒径分布脂质体的整个药代动⼒学过程,如全⾝循环和MPS***、外渗到组织间质、细胞外基质间质运输以及细胞摄取和细胞内运输,都是依赖于尺⼨的。粒径<200nm的颗粒可降低⾎清蛋⽩的调理作⽤,降低MPS的***率。在⼩⿏⽩⾎病模型中,对于Myocet来说,较⼩的脂质体具有更⾼的抗**功效和增加的平均⽣存时间。粒径为2.0-3.5µm的Mepact可促使单核细胞/巨噬细胞吞噬,触发*****的免疫调节作⽤。Singh等⼈发现,含有不同颗粒⼤⼩的佐剂脂质体(ArmyLiposomeFormulation,ALF)的疫苗会产⽣不同的免疫反应,即树突状细胞更有效地摄取10-200nm范围内的⼩颗粒,⽽其他免疫细胞,如巨噬细胞,则倾向于吞噬⼤颗粒。Niu等⼈研究了⼝服给药的胰岛素负载脂质体,发现直径为150nm和400nm的脂质体表现出较慢且持续时间⻓达24⼩时的降糖作⽤,⽽粒径约为80nm和2µm的脂质体则分别表现出短暂且⽆药理作⽤。文献表明,对于*****的脂质体来说,小于200nm的脂质囊泡大小可以从物理肝脏筛选过程中逃逸。根据肝窦的大小,需要小于150nm的囊泡才能通过高渗透性的**血管穿透到恶性组织中。因此,它是由增强的渗透率(EPR)效应控制的,这有助于脂质体通过被动靶向在**中积累。一些常用于标记脂质体的荧光染料包括:DiO、DiI、Rhodamine PE、NBD、BODIPY、Cy3和Cy5等。

脂质体制备方法:破碎技术尺⼨和尺⼨分布是脂质体性能和安全性的关键属性。有⼏种⽅法可⽤于减少脂质体的尺⼨,如(超)超声(通过浴或探针),挤压,均质,或组合⽅法,如冻融挤压,冻融超声和⾼压均质挤压技术。在这些技术中,挤压和⾼压均质(HPH)是在制药制造中**常⽤的技术。⼤尺⼨的脂质体通过聚碳酸酯膜(50nm~5µm)成为粒径分布精细的较⼩的脂质体。众所周知,商业化的纳⽶脂质体产品,包括Onivyde、Vyxeos、Marqibo等,都是采⽤这种⽅法进⾏⽣产的。该⽅法相对简单,重现性好,只需要适中的条件。尺⼨减⼩的潜在机制是MLV在膜孔⼊⼝处破裂,并在膜通过过程中重新排列。关键的⼯艺参数,如聚碳酸酯膜的孔径、通过循环次数、压⼒和流速等,都可以影响脂质体的⼤⼩和⽚层性。Ong等⼈发现,在⽐较其他不同的纳⽶化技术(包括冻融超声、超声和均质化)时,挤出是***的技术。然⽽,挤压可能会降低脂质体的包封性并改变不对称脂质体的结构。HPH⽤于⽣产各种纳⽶制剂,如脂质体、纳⽶晶体和纳⽶乳液。它既适⽤于⽔体系,也适⽤于⾮⽔体系,并提供不同的⽣产规模,从容量为10L/h的实验室规模到容量为10万L/h的⼤型⽣产规模。脂质体质量控制主要包括原材料质量控制、制备工艺参数控制产品特性测试、微生物污染控制和质量标准建立等。福建脂质体载药给药
PAMAM树状大分子偶联,与DOPE(1:1)混合形成脂质体具有细胞核靶向功能。石家庄脂质体载药研发
脂质体被动载药⽅法
被动载药⽅法是在脂质体制备过程中对药物进⾏包封的方法。药物可以通过药物分⼦与脂质之间的共价、离⼦、静电、⾮共价或位阻相互作⽤被包封在内⽔空间内或包埋在脂质体的双层中。这种⽅法的主要缺点是包封效率低,从⽽导致额外的游离药物去除步骤。通过对**和出版物的了解,已上市的采⽤被动载药⽅法的脂质体产品包括AmBisome、Visudyne、Arikayce、DepoCyte、DepoDur和Expel。被动载药⽅法可⽤于亲脂***物物质。例如椎体卟啉,⼜称苯并卟啉衍⽣物单酸环A(BPD)(Vi-sudyne),是⼀种⾼亲脂性分⼦,能有效促进药物参与到脂质双分⼦层中。匀浆后,BPD在脂质体中的包封效率⼏乎为100%。AmpB(AmBisome)由于其两亲性结构,在⽔和⼤多数有机溶剂中难溶。AmpB可以通过带正电的AmpB氨基与带负电的DSPG磷酸基之间的离⼦结合紧密嵌⼊脂质双分⼦层。在pH1.0-3.0的酸性环境中,离⼦相互作⽤很容易形成。此外,AmpB的多烯部分与磷脂的脂肪烃链之间的疏⽔相互作⽤进⼀步加强了这种联系。被动载药法也可以用于亲⽔***物物质。硫酸阿⽶卡星是⼀种⾃由⽔溶性抗***药物。 石家庄脂质体载药研发
上一篇: 中国台湾超声微泡报价
下一篇: 上海超声微泡成像