安徽RNA免疫共沉淀RIP-Sequencing
RIP-qPCR实验技术的原理是基于RNA免疫沉淀(RNA Immunoprecipitation, RIP)与实时荧光定量PCR(quantitative real-time PCR, qPCR)的结合。首先,通过RIP技术,利用抗体特异性地识别并结合目标RNA结合蛋白(RBP),将RBP与其结合的RNA一起沉淀下来。这一步骤依赖于抗体与RBP之间的特异性相互作用,确保只有与目标RBP结合的RNA被沉淀。接下来,从沉淀的复合物中提取RNA,并通过逆转录将其转化为cDNA。然后,利用qPCR技术对特定的RNA分子进行定量检测。在qPCR反应中,通过荧光信号的实时监测,可以准确测量PCR产物的累积量,从而实现对目标RNA的定量分析。综上所述,RIP-qPCR实验技术的原理是通过特异性抗体沉淀目标RBP及其结合的RNA,然后利用qPCR对沉淀下来的RNA进行定量检测。这项技术结合了RIP的特异性和qPCR的灵敏性,为研究细胞内RNA与蛋白质的相互作用提供了有力工具。通过这种方法,可以深入了解RNA与蛋白质在细胞内的结合情况,揭示转录后调控网络的动态过程。如果RIP-qPCR实验失败了,该怎么办。安徽RNA免疫共沉淀RIP-Sequencing

RIP-seq和RIP-qPCR实验都是研究RNA与蛋白质相互作用的实验方法,但存在一些异同点。相同点:两者都基于RNA免疫沉淀(RIP)技术,利用特定蛋白的抗体将RNA-蛋白质复合物沉淀下来,以研究RNA与蛋白质的相互作用。两者都需要对实验条件进行优化,以确保实验的特异性和准确性。不同点:实验目的:RIP-seq主要用于筛选与目标蛋白结合的未知RNA,绘制全基因组范围的RNA与蛋白质相互作用图谱,而RIP-qPCR则用于验证与目标蛋白结合的已知RNA。数据分析:RIP-seq产生高通量测序数据,需要生物信息学分析以识别与蛋白质结合的RNA序列;而RIP-qPCR产生定量PCR数据,通过相对定量方法分析特定RNA与蛋白质的结合情况。应用范围:RIP-seq更适合于发现新的RNA与蛋白质的相互作用,并研究其在全基因组范围内的分布和特征;而RIP-qPCR更适用于特定RNA与蛋白质相互作用的验证和定量研究。总之,RIP-seq和RIP-qPCR实验在研究RNA与蛋白质的相互作用时各有优势,研究者可根据具体需求选择合适的方法。天津互作机制RIP-SequencingRIP实验旨在精确地研究目标RNA与特定蛋白质的相互作用,实验设计有哪些关键步骤。
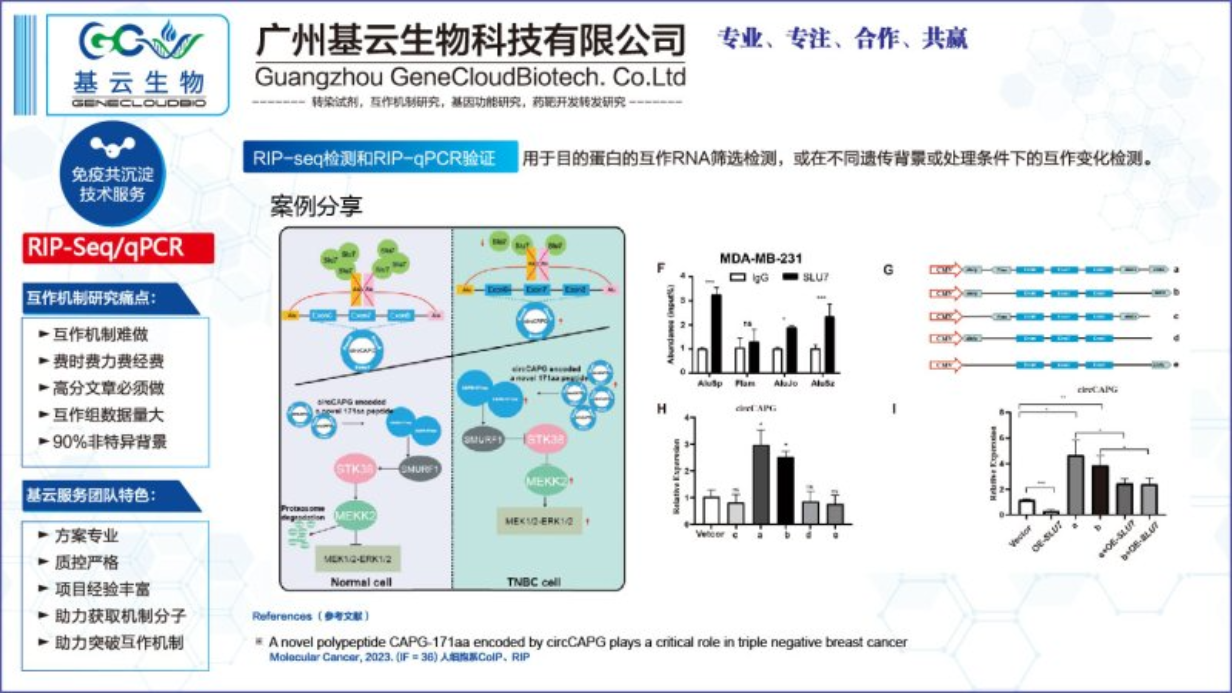
进行RIP-qPCR实验的主要目的是研究和验证特定蛋白质与RNA分子之间的相互作用。这项技术结合了免疫沉淀(用于捕获蛋白质-RNA复合物)和实时荧光定量PCR(用于定量检测特定RNA分子的表达水平),从而提供了一种有效手段来分析细胞内蛋白质与RNA的结合情况。通过RIP-qPCR实验,研究人员可以识别与特定蛋白质结合的RNA分子,进一步了解这些RNA分子在细胞内的功能、定位以及调控机制。这种相互作用的分析对于深入理解转录后调控、RNA稳定性、剪接变体选择以及非编码RNA的功能等生物学过程至关重要。此外,RIP-qPCR还可用于验证其他实验结果,如基因表达谱、蛋白质组学或生物信息学分析所揭示的潜在蛋白质-RNA相互作用。通过结合多种实验方法,研究人员可以获得更详细的细胞调控网络视图,为疾病机制的研究和新药开发提供有力支持。总之,RIP-qPCR实验的目的在于揭示细胞内蛋白质与RNA的相互作用关系,深化我们对基因表达调控和细胞功能的认识,并为生物医学研究提供有价值的实验依据。
进行RIP实验时,抗体的选择是实验成功的关键之一。以下是选择抗体时需要考虑的几个要点。1. 特异性:首要考虑的是抗体的特异性。必须选择能够特异性识别并结合目标蛋白的抗体,以避免非特异性结合和背景噪音。可以通过查阅文献、抗体供应商提供的数据或进行预实验来验证抗体的特异性。2. 亲和力:抗体的亲和力也是重要的考虑因素。高亲和力的抗体能够更紧密地结合目标蛋白,提高免疫沉淀的效率。可以选择经过验证的高亲和力抗体,或者通过预实验比较不同抗体的结合能力。3. 物种来源和反应性:根据实验需求选择适当的抗体物种来源和反应性。确保抗体能够与样本中的目标蛋白发生特异性反应,同时避免与其他非目标蛋白发生交叉反应。4. 兼容性:考虑抗体与实验流程的兼容性。某些抗体可能不适用于特定的实验条件或步骤,因此在选择抗体时需要仔细查阅抗体说明书和实验方案。综上所述,进行RIP实验时,应选择具有高特异性、高亲和力、适当物种来源和反应性,以及与实验流程兼容的抗体。通过仔细评估和选择抗体,可以提高实验的准确性和可靠性。RIP-seq主要应用于识别和分析与特定RNA结合蛋白(RBP)结合的RNA分子。
RIP-qPCR实验(RNA Immunoprecipitation followed by quantitative PCR)是一种用于研究细胞内特定蛋白质与RNA相互作用的技术。该技术结合了免疫沉淀(Immunoprecipitation)和实时荧光定量PCR(quantitative PCR,qPCR)的方法,旨在识别和定量与特定蛋白质结合的RNA分子。在RIP-qPCR实验中,首先使用针对目标蛋白质的特异性抗体进行免疫沉淀,将与该抗体结合的蛋白质-RNA复合物从细胞裂解液中分离出来。随后,通过洗涤步骤去除非特异性结合的分子,保留与目标蛋白质特异性结合的RNA。接下来,从免疫沉淀复合物中提取RNA,并将其逆转录为cDNA。然后,利用特异性引物进行qPCR反应,以定量检测与目标蛋白质结合的特定RNA分子的丰度。通过比较不同样品中目标RNA的相对表达水平,可以评估蛋白质与RNA之间的结合强度和特异性。RIP-qPCR实验在生物学研究中具有广泛应用,可用于研究转录后调控、RNA转运、RNA稳定性以及非编码RNA与蛋白质相互作用等方面的问题。该技术为揭示细胞内基因表达调控的复杂网络提供了有力工具。做好RIP实验,应注意哪些常见问题。安徽RNA免疫共沉淀RIP-Sequencing
RIP-qPCR实验技术具有多个优点和一些潜在的缺点。安徽RNA免疫共沉淀RIP-Sequencing
如果RIP-qPCR实验失败了,首先不要过于沮丧,因为实验失败在科学研究中是常有的事情。重要的是要冷静分析失败的原因,并采取相应的措施来解决问题。首先,回顾实验过程,检查是否有操作失误或疏忽。例如,检查引物设计是否合理、试剂是否过期、加样是否准确等。这些细节问题都可能导致实验的失败。其次,分析实验数据,看看是否有异常值或不符合预期的结果。这可能是由于实验条件设置不当、样本质量不佳或仪器故障等原因造成的。根据数据分析结果,可以调整实验条件或重新准备样本进行再次实验。另外,寻求他人的帮助和建议也是一个好的选择。可以向实验室的同事、导师咨询,他们可能会提供有价值的建议和解决方案。总结经验教训,避免再次犯同样的错误。实验失败也是一种学习的机会,通过分析失败的原因和采取相应的改进措施,可以提高实验技能和科学素养。总之,面对RIP-qPCR实验的失败,要保持冷静、分析原因、寻求帮助并总结经验教训。相信通过不断的努力和学习,终会取得成功。安徽RNA免疫共沉淀RIP-Sequencing
下一篇: 安徽染色体免疫沉淀检测ChIP