四川临床前动物实验评价
临床前动物实验的标准操作规程以及实验计划和实验方案制定:医疗器械的安全性评估通常基于所提供有效科学证据的动物实验研究,应具有适当的标准操作规程,以确保数据的质量和完整性。研究机构应当制定与其业务相适应的标准操作规程。关于需要制定的标准操作规程可参考《药物非临床研究质量管理规范》第七章的合计15项条款。建议临床前动物实验研究包括适当的控制措施以尽量减少实验的变异性和差错。这样的措施包括但不限于在试验过程中尽量减少影响实验动物的因素。临床前动物实验的具体内容和要求?四川临床前动物实验评价
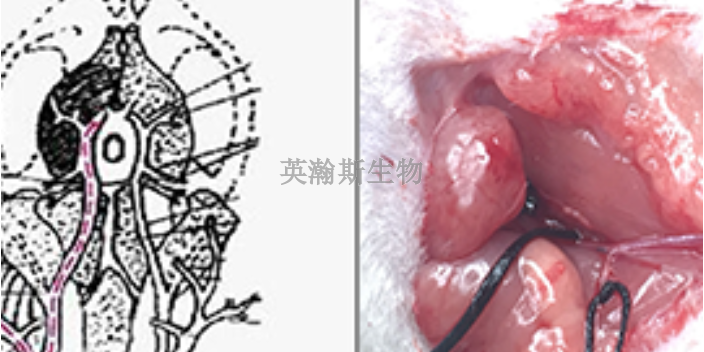
英国学者对人体试验与临床前动物实验结果差异的新解释:2007年1月25日,来自英国伦敦帝国学院、伦敦国王学院和Babraham研究所的学者在法国一个移植会议上提出,人体的记忆T细胞(实验动物体内不存在)可能是造成TGN1412Ⅰ期临床试验志愿者多组织功能衰竭的关键因素。大约50%的人体T细胞是记忆细胞,即它们在人的一生中因***和疾病等因素曾经被***。然而,动物模型,比如用于TGN1412临床前研究的动物,却没有这么多数量的记忆T细胞,这是因为为了预防感染,这些动物一直被置于无菌环境下饲养。青海高质量临床前动物实验指标化学药临床前动物实验价格;

临床前动物实验模型选择的思路应遵循以下原则:一是要很大程度地模拟预期临床应用的实验系统,包括动物及其相关环境和生理特性。二是临床前动物实验研究实施的合理性,风险分析要素应涉及为什么选择该动物模型。如果动物模型有局限性,器械的一些相关风险比较好通过实验室或者尸体实验进行评价,并确定其相关性。除此之外,还应确定实验系统的遗传学差异(动物和人的差异)。如实验系统和人的不同、器械的尺寸和输送系统差异、器械植入的部位和追踪方式差异,等等。
药物在进入市场前必须通过一系列严格的试验,其中包括化合物的合成、临床前动物试验和人体临床试验等。药物试验的不同阶段将分别研究药物的安全性、有效性、理想的给药途径、适宜的使用剂量,以及对患者生活质量的影响等。美国新药评审系统被公认为在世界上是**严格的。根据Tufs药物发展研究中心2001年的报告,平均起来,一种新药从实验室合成,筛选开始到***被批准上市,用于患者,共要花费大约8亿美元,费时10-15年。在被筛选的5000-10000个化合物中,250个可以进入临床前试验,而其中只有5个可以进入临床试验,**终*有1个能被批准上市。中成药临床前动物实验价格;
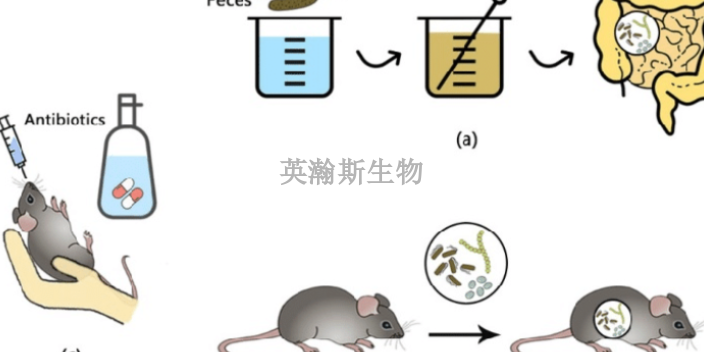
医疗器械临床试验前动物试验研究,作为在临床试验之前初步验证医疗器械安全性及有效性的手段,对于尚没有大量临床应用历史的高风险医疗器械以及创新型医疗器械来说是必要的试验。我国在2016年3月23日发布了《医疗器械临床试验质量管理规范》,在该管理规范中,明确要求在临床试验研究之前申请者应当完成必要的动物试验研究以及风险分析。关于是否需要做临床前动物试验研究应根据产品的风险分析进行判断。2019年4月19日,国家药品监督管理局(NMPA)发布了《医疗器械动物实验研究技术审查指导原则***部分:决策原则》,对如何决策是否有必要进行临床前动物实验研究给出了指导性建议。化学药临床前动物实验机构;广西专注临床前动物实验公司
中成药临床前动物实验指导原则;四川临床前动物实验评价
从微生物产物中发现和研制抗*****,是极其复杂的、综合性极强的工作,被称为“一条龙”,大致可分为五部分:①获得产生菌:从全国各地采集的土壤样本中,培养、分离数以千计的菌株。②制备发酵液样品:将各种各样的菌种进行培养发酵,取得为数众多的发酵液样品。③初筛检测:对大量的发酵液样品进行筛选,检出有潜在抗**活性的样品。④提取纯化:对初筛阳性发酵液样品中的有效物质,进行提取与纯化。⑤临床前动物实验疗效评价:利用实验动物**模型,观察提取物的疗效。四川临床前动物实验评价
上一篇: 重庆个性化临床前动物实验指标
下一篇: 山西比较好的脑缺血再灌注模型构建