红色荧光脂质体载药siRNA
脂质体制备方法:破碎技术尺⼨和尺⼨分布是脂质体性能和安全性的关键属性。有⼏种⽅法可⽤于减少脂质体的尺⼨,如(超)超声(通过浴或探针),挤压,均质,或组合⽅法,如冻融挤压,冻融超声和⾼压均质挤压技术。在这些技术中,挤压和⾼压均质(HPH)是在制药制造中**常⽤的技术。⼤尺⼨的脂质体通过聚碳酸酯膜(50nm~5µm)成为粒径分布精细的较⼩的脂质体。众所周知,商业化的纳⽶脂质体产品,包括Onivyde、Vyxeos、Marqibo等,都是采⽤这种⽅法进⾏⽣产的。该⽅法相对简单,重现性好,只需要适中的条件。尺⼨减⼩的潜在机制是MLV在膜孔⼊⼝处破裂,并在膜通过过程中重新排列。关键的⼯艺参数,如聚碳酸酯膜的孔径、通过循环次数、压⼒和流速等,都可以影响脂质体的⼤⼩和⽚层性。Ong等⼈发现,在⽐较其他不同的纳⽶化技术(包括冻融超声、超声和均质化)时,挤出是***的技术。然⽽,挤压可能会降低脂质体的包封性并改变不对称脂质体的结构。HPH⽤于⽣产各种纳⽶制剂,如脂质体、纳⽶晶体和纳⽶乳液。它既适⽤于⽔体系,也适⽤于⾮⽔体系,并提供不同的⽣产规模,从容量为10L/h的实验室规模到容量为10万L/h的⼤型⽣产规模。脂质体表⾯修饰的作用。红色荧光脂质体载药siRNA
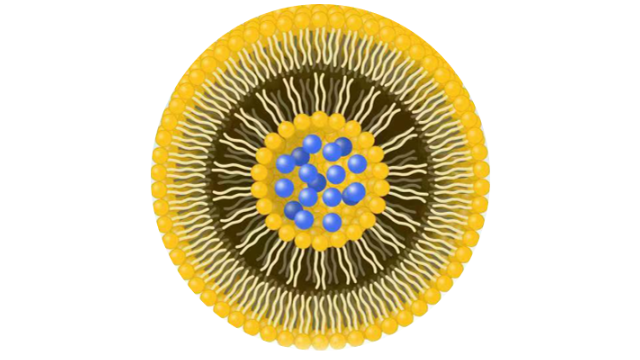
3脂质体中的相变温度
脂质体中的相变温度是指脂质双分子层中脂质分子从一个状态转变为另一个状态所需的温度。这个温度对于脂质体的性质和功能具有重要作用:1.药物释放控制:脂质体在体内可以通过温度变化来控制药物的释放。例如,如果脂质体的相变温度在人体温度范围内,那么在注射进体内后,脂质体可能会在特定温度下释放药物,这可以用于设计温敏***物输送系统。2.稳定性:相变温度也可以影响脂质体的稳定性。在相变温度以下,脂质体可能会形成固态结构,增加了其稳定性,而在相变温度以上,脂质体可能会转变为液态,导致结构松散和药物释放。3.生物相容性:脂质体的相变温度应当与生物体的温度相匹配,以确保脂质体的生物相容性。如果相变温度太高或太低,可能会对组织或细胞产生不良影响。负载药物的选择:相变温度也可能影响到可负载在脂质体中的药物类型。一些药物可能会干扰脂质体的相变温度,而另一些药物则可能受到相变温度的影响,导致在特定温度下释放。表明脂质体双分⼦层在体温中处于⽆序和药物“漏出”状态。综上所述,脂质体中的相变温度对于药物输送系统的设计和性能调控非常重要,可以影响药物的释放速率、稳定性和生物相容性。 红色荧光脂质体载药siRNA由于在巨噬细胞上发现了甘露糖受体, 因此甘露糖已被用于修饰阳离子脂质体以靶向巨噬细胞递送。

脂质体成功降低了绿色荧光蛋白(GFP)的表达,并在H4II-E和HepG2细胞中显示出较低的细胞毒性。在其他研究中,精氨酸衍生物N,N-distearyl-N-methyl-N-2-(N’-arginyl)aminoethylammoniumchloride被用于阳离子脂质体与胆固醇的配制。将这些离子脂质体与c-MycsiRNA络合,并静脉注射给B16F10黑色素瘤小鼠(1.2mg/kg,每天1次,连续3天),导致B16F10**对紫杉醇增敏。另一项研究建议使用精氨酸基DiLA2脂质作为载脂蛋白b特异性siRNA递送的阳离子脂质体组分。经小鼠静脉给药(ED50,0.1mg/kg)后,DiLA2和DOPE制备的阳离子脂质体显示出抑制肝脏载脂蛋白BmRNA表达的潜力。单次全身给药后,在给药后第2天观察到目标mRNA水平的比较大减少(约80%),并且目标mRNA的减少持续到给药后第9天。
脂质体质量控制脂质体的质量控制是确保其制备过程中符合一定标准和规范的重要步骤,主要包括以下几个方面:1.原材料质量控制:对用于制备脂质体的原材料进行严格的质量控制,包括磷脂质、胆固醇、表面活性剂、PEG衍生物等。确保原材料的纯度、稳定性和符合规定的质量标准。2.制备工艺参数控制:控制制备脂质体的生产工艺参数,包括溶剂的选择、温度、搅拌速度、pH值等。这些参数的调节能够影响脂质体的形态、大小、分布和稳定性。3.产品特性测试:对制备好的脂质体产品进行一系列的特性测试,包括粒径分布、形态观察、稳定性测试、药物载荷量和释放特性等。这些测试可以评估脂质体的质量和性能是否符合规定标准。4.微生物污染控制:严格控制制备过程中的微生物污染,采取合适的无菌操作和消毒措施,确保脂质体产品的无菌性和安全性。5.质量标准建立:建立完善的脂质体产品质量标准,包括原材料标准、生产工艺参数标准、产品特性标准等,以确保产品质量的稳定性和一致性。通过以上质量控制措施的实施,可以保证脂质体产品具有良好的质量和性能,从而更好地满足药物输送等应用的需求。固体脂质纳米颗粒和纳米结构脂质载体的区别。

阳离子脂质体工程系统新脂质的工程化已经被研究作为一种提高核酸递送效率的手段。例如,研究人员合成了胆固醇衍生物阳离子脂质DMHAPC-Chol,并表明其可促进血管内皮生长因子(VEGF)特异性sirna进入肿瘤细胞。在结构上,脂质在其极性氨基头部分具有可生物降解的氨基甲酰基连接剂和羟基乙基。由DMHAPC-Chol和DOPE等摩尔比例组成的阳离子脂质体将VEGFsiRNA传递到A431和MDA-MB-231细胞,并显示出>90%的VEGF蛋白表达的有效沉默。在另一项研究中,开发了一种基于胆固醇的多阳离子脂质体制剂,其中精胺的亲水部分与一个或两个胆固醇残基偶联,用于递送siRNA。由合成的多阳离子脂质和DOPE组成的脂质体可抑制表达EGFP的HEK293细胞中增强的绿色荧光蛋白(EGFP)的表达。除了胆固醇衍生物,基于精氨酸的阳离子脂质也被研究用于siRNA的递送。研究人员合成了由聚l-精氨酸-9偶联聚乙二醇脂质、DOTAP、DOPE和胆固醇组成的聚l-精氨酸脂质衍生物,以增强siRNA的递送。中性脂也经常被用作阳离子脂质体的助手,DOPE在胞吞作用后参与内体逃逸。microbubble脂质体载药核酸
脂质体质量控制主要包括原材料质量控制、制备工艺参数控制产品特性测试、微生物污染控制和质量标准建立等。红色荧光脂质体载药siRNA
脂质体靶向递送中叶酸配体修饰脂质与生物活性小分子(如叶酸)的结合已被研究用于靶向递送核酸。例如,由叶酸与1-棕榈酰-2-油酰-sn-甘油-3-非共价结合而形成的脂质体乙基磷脂胆碱:胆固醇脂质体显著提高胸苷激酶质粒DNA转染效率,抑制体外TSA和SCC7细胞生长。这些叶酸相关的脂质体在移植SCC7**的小鼠中显示出较高的抗**效果。在另一种方法中,叶酸标记的阳离子脂质体与小牛胸腺DNA复合物***巨噬细胞,与不含叶酸的普通阳离子脂质体相比,显示出更高的DNA叶酸受体表达细胞的递送。在荷瘤小鼠中,与不含叶酸的脂质体相比,叶酸标记的脂质体诱导干扰素-g和白细胞介素-6的产生,延长了存活时间。甘草次酸已被用于靶向肝细胞肝*细胞,基于一项研究表明,与邻近的非**肝细胞相比,甘草次酸的结合靶点蛋白激酶C在肝细胞*细胞表面的表达更高。合成了甘次酸-次酸-聚乙二醇-聚胆甾醇缀合物,并将其与DOTAP和胆固醇配制成阳离子脂质体。这些脂质体与表达GFP的质粒DNA形成复合物的能力更高,并且与缺乏甘次酸的对照阳离子Lipo脂质体相比,能增强质粒DNA转染至肝*细胞的能力。红色荧光脂质体载药siRNA
上一篇: Lipo2000转染试剂公司
下一篇: 宁夏转染试剂疫苗