多重免疫组化
直接免疫荧光:单抗体(一抗)用于免疫染色和检测目标蛋白。荧光素结合的一抗直接与目标抗原结合,并使用成像显微镜观察。直接免疫荧光的优点:由于无需为两种抗体选择不同的物种反应性,从而降低了物种交叉反应性问题。与间接免疫荧光相比,时间缩短(操作步骤减少)。直接免疫荧光的缺点:不允许通过二抗进行信号放大;检测灵敏度降低;荧光素结合一抗的选择有限;与使用荧光二抗的检测相比,更昂贵。间接免疫荧光:使用两种抗体(一抗和二抗)进行免疫染色并检测目标蛋白。首先,用特异性一抗标记目标蛋白。然后,荧光素结合的二抗(与一抗具有不同的物种反应性)识别结合的抗原-抗体复合物并与一抗结合。由于一个以上的二抗可以与一抗结合,荧光信号被放大,提供了更高的检测灵敏度。荧光抗体技术可用于检测和定位各种抗原,也可以用于检测和定位抗体。多重免疫组化
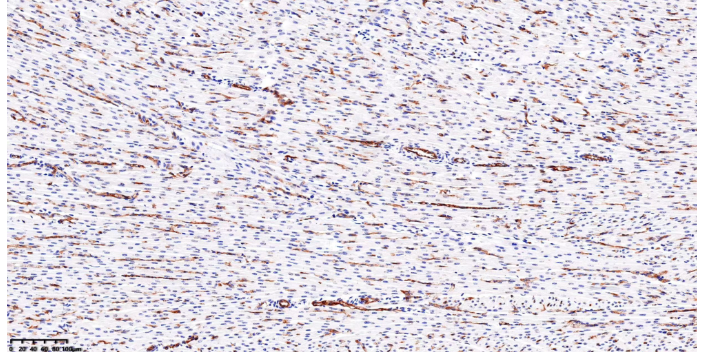
细胞免疫荧光步骤是什么呢?步骤:1. 细胞一定要贴在玻片上(较好可以放入24孔板),为后面照像打基础。细胞密度适中,大约60-75%满片即可,否则容易脱片。2. 取出细胞后用4%多聚甲醛固定15分钟,现用现配。(以下各步骤切毋使玻片干燥)3. PBS冲洗;4. 0.1%Triton作用20分钟;5. PBS冲洗;6. 10%正常血清封闭10分钟;7. 加入一抗,4度孵育过夜(找个小瓶盖将小玻片支起来,抗体就不容易溢出),还要记住“砸片”,就是抗体从较高处落到片子上,以分布均匀。抗体稀释度1:60,较常用!8. PBS冲洗4次,各5分钟;9加入荧光二抗,室温30分钟。抗体稀释度1:400,较常用!10. 90%甘油封片。也很关键阿,多封几次才有体会。12. 避光保存,或到显微镜下观察。多重免疫组化免疫荧光技术可以用于研究动物模型和药物筛选。
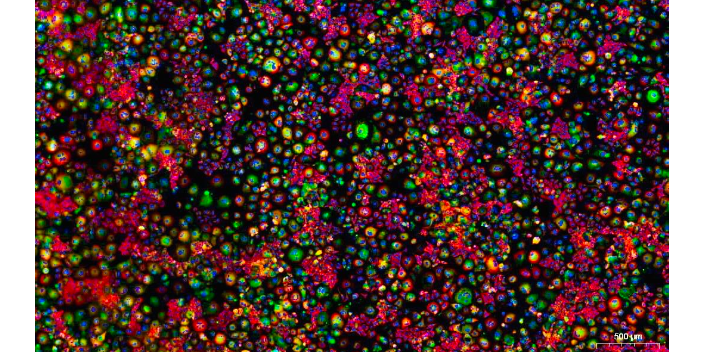
细胞免疫荧光实验注意事项:非特异性染色:是否灭活内源性过氧化物酶;孵育过程中干片;抗原热修复过度。染色过深:一抗浓度过高;染色试浓度过高或孵育时间过长;染色剂浓度过高或孵育时间过长。通常实验室先固定细胞再进行通透,但若检测抗原是水不溶性蛋白,可先通透再固定,这样可以通过通透去除一些水溶性蛋白,进而可降低免疫荧光背景和非特异性信号;建议设阴性对照组,消除由于抗体非特异性结合而产生的背景染色;选择醛类固定液时,保持其新鲜度,较好现配现用,使用不新鲜的醛类固定液自发荧光背景会升高。
免疫荧光固定(防止离体组织自溶抗原扩散),固定液包括:有机溶剂(甲醇、乙醇等);交联剂(4%PFA、10%中性福尔马林),固定液的选择取决于被研究抗原的性质及所用抗体的特性,不过,目前甲醛用的还是较多的,但针对磷酸化的抗体,不适合用甲醛,会导致磷酸蛋白从膜表面转移到胞浆中,故应选择冰冷的无水甲醇或无水乙醇,同时应注意甲醛会挥发,在4-8°C不宜储存太久。固定时间:取决于组合块的大小和类型,对于大多数组织,18-24h较为理想,细胞固定时间较短,一般2%的甲醛室温固定20min即可。以细胞样品为例:用4%的多聚甲醛固定爬片15min,PBS浸洗玻片3次,每次3min。免疫荧光技术可以用于研究药物的靶点和作用机制。

荧光标记二抗的选择普遍;与使用荧光素结合一抗的检测相比,成本较低。间接免疫荧光的缺点:由于需要具有两种不同物种反应性的两种抗体,因此物种交叉反应性问题增加;与直接免疫荧光相比,时间更长(操作步骤更多)。间接免疫荧光的优点:通过增加能够与一抗结合的二抗数量进行信号放大;与直接免疫荧光相比,通过信号放大提高检测灵敏度;荧光标记二抗的选择普遍;与使用荧光素结合一抗的检测相比,成本较低。间接免疫荧光的缺点:由于需要具有两种不同物种反应性的两种抗体,因此物种交叉反应性问题增加;与直接免疫荧光相比,时间更长(操作步骤更多)。免疫荧光技术可以用于研究植物病理学和农业生产。多重免疫组化
免疫荧光技术可以同时检测多个目标分子,通过不同颜色的荧光染料进行标记。多重免疫组化
免疫荧光间接法:如检查未知抗原,先用已知未标记的特异抗体(一抗体)与抗原标本进行反应,用水洗去未反应的抗体,再用标记的抗抗体(第二抗体)与抗原标本反应,使之形成抗体—抗原—抗体复合物,再用水洗去未反应的标记抗体,干燥、封片后镜检。如果检查未知抗体,则表明抗原标本是已知的,待检血清为一抗体,其它步骤的抗原检查相同。标记的抗抗体是抗球蛋白抗体,同于血清球蛋白有种的特异性,如免疫抗鸡血清球蛋白只对鸡的球蛋白发生反应,因此,制备标记抗体适用于任何抗原的诊断。多重免疫组化
上一篇: 南京油红O扫描成像工具
下一篇: 济南tunel扫描仪