医疗器械委托加工
生产阶段:《总局办公厅关于医疗器械产品技术要求有关问题的通知》中明确规定:企业应当根据产品技术要求、产品特性、生产工艺、生产过程、质量管理体系等确定生产过程中各个环节的检验项目,以产品检验规程的形式予以细化和固化,用以指导企业的出厂检验和放行工作,确保出厂的产品质量符合强制性标准以及经注册或者备案的产品技术要求。生产过程中的质量控制措施的实施(如:入场检验、过程检验、出厂检验等)、作业指导书的制定、原材料的要求等很大程度上都是来源于产品技术要求。设计和开发输入应具体、明确和充分,包括用户对产品的要求、法规和标准的分析以及风险管理。医疗器械委托加工

医疗产品的设计肩负着巨大的责任。因为我们正在开发的以及已经投入市场的产品,全世界数百万人每天都在与之互动。那是些完全有机会改变和拯救生命的产品。这些产品可能在市场上市几年或更长时间,时时刻刻影响着人们管理自己的健康或他人的健康的方式。因此,医疗产品设计人员必须做出经得起时间考验的决定,这样才能设计出适合较为用户群体的产品。我们如何确保我们所做的决定能产生设计良好的产品?医疗产品设计领域的出现并非是一蹴而就的,它也经历了时间的沉淀。医疗器材设计思脉得,为医疗器械企业提供从研发转发到上市的CDMO+CRO+CMO一站式解决方案。
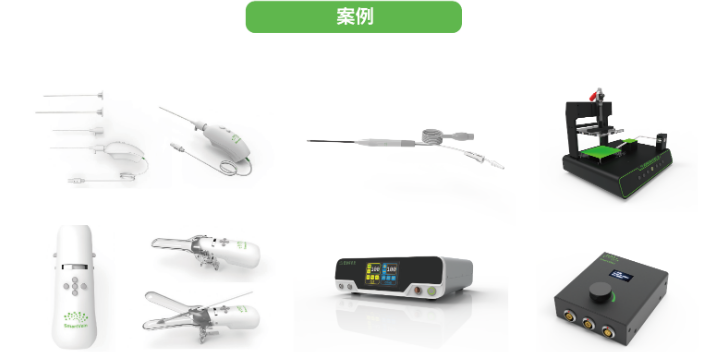
设计开发计划中的资源包括生产场地、生产设备、关键原材料的获取、设计开发人员,一般包括结构工程师(设计产品外观和结构)、电子工程师(电路板设计)、软件工程师(软件开发会随着产品复杂程度的增加)。按照人机料法环测的六大要素进行分析。生产现场:需要无尘车间和洁净车间;生产设备:满足产品制造要求的能力;生产方式:产品的生产工艺是否难以实现;测试设备:测试产品的某些性能;人员素质:具备相应能力的人。结构工程师、电子工程师、软件工程师、检测人员等等。
设计确认:设计确认是指通过提供客观证据,确认产品的特定预期用途或使用要求已得到满足。设计确认的内容:R&D部负责修改和补充图纸、设计文件、工艺文件等。根据试制、测试的要求,已知产品的预期用途和提出的改进建议,进而确认产品的设计。设计确认包括产品标准、临床文献、性能评价数据、工艺文件、原料质量标准、产品说明书和包装标签、试制和试验记录、试验过程的原始数据和记录、产品安全性、风险评估、可靠性等。、满足顾客要求和国家法律法规及国家标准要求的程度。医疗器械设计开发哪家好-推荐咨询思脉得(嘉兴)医疗科技有限公司!
软件开发过程要求:做好软件准备管控,确保软件设计开发全过程可追溯。企业应根据《规范》要求建立软件配置管理档案,有能力和条件的可以使用CVS、VSS等相关软件。企业应为每个软件版本建立统一的基线,包括规格、软件代码、打包的现成软件等。目前在审计中发现,在软件设计过程中,企业随意控制软件版本,开发过程版本与官方发布版本的对应性不强。企业应关注软件注册规定中的版本要求,并根据自身情况规范软件版本管理和更新要求。医疗器械产品的设计开发过程是需要进行质量控制的重要环节,无论是标准还是法规都对产品的设计开发有要求。医用设备设计
在质量管理体系中,设计和开发是非常关键和重要的质量管理过程。医疗器械委托加工
医疗器械的生命周期主要包括8各阶段,每个阶段的工作和主意事项也不尽相同。主要包括1)计划阶段;2)设计输入阶段;3)设计输出阶段;4)产品试制阶段;5)设计验证阶段;6)设计确认阶段;7)设计转换报告;8)风险管理报告。因为医疗器械重视过程记录和闭环控制管理,所以对每个医疗器械产品的要求都不一样。但是每个阶段都有相应的设计文档。设计验证和设计确认这两个阶段是不同的。不同的是,设计验证阶段主要是确认产品是否满足用户需求,而设计验证的目的是是否覆盖了设计输入中的所有条目。设计包括产品型式试验和各种性能试验。医疗器械委托加工
思脉得(嘉兴)医疗科技有限公司致力于医药健康,是一家服务型的公司。思脉得医疗集团致力于为客户提供良好的技术服务,注册服务,产品服务,制造服务,一切以用户需求为中心,深受广大客户的欢迎。公司将不断增强企业重点竞争力,努力学习行业知识,遵守行业规范,植根于医药健康行业的发展。思脉得医疗集团立足于全国市场,依托强大的研发实力,融合前沿的技术理念,及时响应客户的需求。
上一篇: 杭州医疗器械设计开发报价
下一篇: 医疗器械生产管理系统