浙江医疗器械设计开发经验丰富
在产品注册阶段,《医疗器械注册申报资料要求和批准证明文件格式》(2014年43号公告)、《总局办公厅关于医疗器械产品技术要求有关问题的通知》以及《医疗器械监督管理条例》中有明确规定:医疗器械产品的备案或注册必须提交产品技术要求文件。在注册技术审评过程中,产品的技术要求是医疗器械技术审评机构的重要关注点。产品的技术要求是否符合适用强制性标准的要求,性能指标的合理性,检验方法的重复性和可操作性,注册的临床评价是否与产品的性能要求等效,是技术审评的重点内容。医疗器械技术评价机构根据产品的技术要求和其他注册资料,对其安全性、有效性研究和结果进行系统评价,并提出结论性的评价意见。设计开发转化过程中,需要确保每个规范都能正确转化为与产品实现相关的具体过程或程序。浙江医疗器械设计开发经验丰富
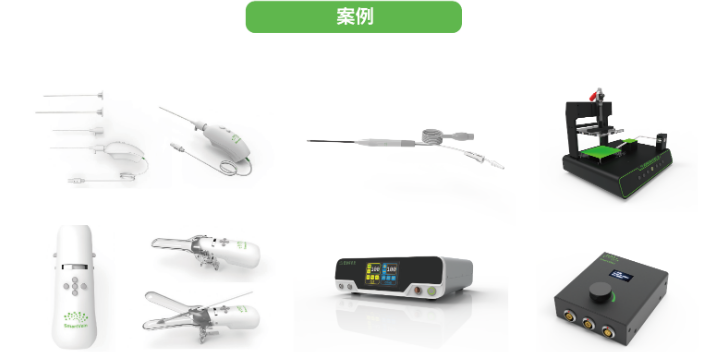
医疗器械的设计和开发过程是一个类似于设定假设、收集数据以证明假设和判断假设的过程。在设计开发输入阶段,首先需要确定产品的功能、性能、界面等要求,形成能够满足临床需求假设的具体产品。然后收集开发产品数据以确定假设。为避免可能引入干扰假设判断的主观因素等,在设定假设时,就应明确范围和要求。在产品性能评估中,输入需要注意两方面的需求:(1)输入必须是明确的需求,在设计开发过程中要保持需求的统一性,避免出现性能评估不一致、设计偏差等逻辑错误。(2)输入应充分收集现有数据,以减少重复实验的实施,从而提高评估质量和效率。医疗器具设计医疗器械设计开发过程中需要严格遵守FDA等监管机构的标准和法规。

医疗器械的安全性和有效性直接关系到用户的健康和生命安全。为确保医疗器械生产企业能够持续稳定地提供满足临床需求、质量合格的产品,需要在质量管理体系的控制下对产品研发和生产的相关过程进行有效运行。监管法规和质量管理体系标准要求设计和开发过程作为产品实现的重要组成部分。输入为产品设计开发提供依据和依据,决定了产品结构、生产工艺、性能评价体系的输出等内容,设计开发输入不仅影响产品的开发和生产,而且在产品开发中起着重要的作用。
医疗器械设计开发确认的关键点就是要确保产品能够满足规定的适用要求,依据所策划并文件化的安排对设计和开发进行确认。思脉得医疗科技技术开发团队凭借过硬的技术储备和专业知识,可以提供指导服务,帮助客户确认产品的合理性。作为设计开发的一部分,还可协助客户按照适用的法规要求进行临床评价或性能评价。如果预期用途需要医疗器械与其他医疗器械连接或结合,还需要确认包含此连接或接合时,证实规定的适用要求或预期用途已得到满足的内容。设计开发团队需要具备医学、生物学、材料学等学科知识背景。
在医疗器械设计输出阶段,需要在设计控制程序下转换为工程设计规范。需要满足设计和开发输入的要求;给出采购、生产和服务适当的信息;包含或引用产品接受准则;规定对产品的安全和正常使用所必需的产品效果;使用CAD和2D工程图创建详细的产品规格。此时,小型仪器转移到制造中,使用具有商业代表性的材料和方法来生产工程原型样机。医疗器械设计中很重要的一步就是设计方案认证和确定,以此来明确仪器设备的制定是不是能达到商品规定和客户要求,向监管部门递交详细的活动报告。尽管监管部门的准许通常出现在医疗设备开发设计的末尾,但应在初期环节考虑到方案设计。选对合作伙伴,可以快速提升医疗器械研发设计能力。电子内窥镜光学测试
医疗器械设计开发需要时刻关注产品的安全性、有效性和质量。浙江医疗器械设计开发经验丰富
确定医疗器械设计和开发输入应该包含哪些内容呢?依据预期的用途、功能、性能、可用性和安全要求;适用的法规要求和标准;适用的风险管理输出;适当时,以前类似设计提供的信息;产品设计和开发所必须的其他要求。需要对如上这些输入的充分性和适宜性进行评审并批准。此外,要求上述内容应保证内容完整、明确,能被验证或确认,并且不能自相矛盾。在设计开发输入阶段定义了医疗器械研发过程中要执行的方法、所需要的仪器、要遵循的过程、要准备的文件以及制造医疗器械的方法。浙江医疗器械设计开发经验丰富
上一篇: 上海电子内窥镜测试设备
下一篇: 医疗器材产品设计