P-AKT 1/2/3免疫荧光检查
细胞免疫荧光实验注意事项:非特异性染色:是否灭活内源性过氧化物酶;孵育过程中干片;抗原热修复过度。染色过深:一抗浓度过高;染色试浓度过高或孵育时间过长;染色剂浓度过高或孵育时间过长。通常实验室先固定细胞再进行通透,但若检测抗原是水不溶性蛋白,可先通透再固定,这样可以通过通透去除一些水溶性蛋白,进而可降低免疫荧光背景和非特异性信号;建议设阴性对照组,消除由于抗体非特异性结合而产生的背景染色;选择醛类固定液时,保持其新鲜度,较好现配现用,使用不新鲜的醛类固定液自发荧光背景会升高。免疫荧光技术可以用于研究食品安全和生物安全。P-AKT 1/2/3免疫荧光检查
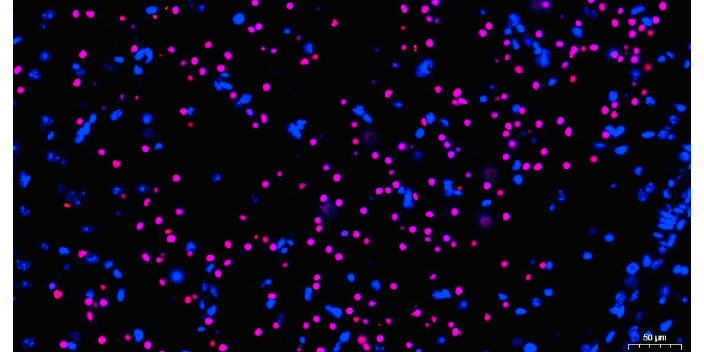
细胞免疫荧光实验常见问题:1、信号弱或者无信号:细胞或组织样本保存时间过长;2)抗体浓度不合适,参照抗体说明书的稀释浓度,再根据样本表达量进行摸索;3)一抗孵育时间不合适,建议 4 ℃ 过夜孵育。2、高背景:封闭不充分;抗体浓度过高;抗体孵育时间过长或温度过高;清洗不充分;样本变干,染色过程确保样品始终浸没于液体环境中.3、非特异性染色较多:固定液残留,这里需要缩短固定时间并且在封闭液中加甘氨酸,并且抗原修复也可以帮助解决非特异性染色;二抗残留,二抗需要用带有吐温 20 的 PBS 溶解,只要荧光显微镜的强度还可以增大,那么就可以增加吐温洗脱掉非特异性染色。P-AKT 1/2/3免疫荧光检查免疫荧光技术可以用于研究动物模型和药物筛选。
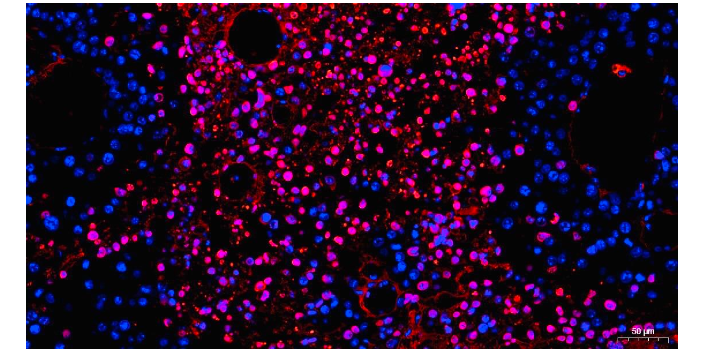
免疫荧光固定(防止离体组织自溶抗原扩散),固定液包括:有机溶剂(甲醇、乙醇等);交联剂(4%PFA、10%中性福尔马林),固定液的选择取决于被研究抗原的性质及所用抗体的特性,不过,目前甲醛用的还是较多的,但针对磷酸化的抗体,不适合用甲醛,会导致磷酸蛋白从膜表面转移到胞浆中,故应选择冰冷的无水甲醇或无水乙醇,同时应注意甲醛会挥发,在4-8°C不宜储存太久。固定时间:取决于组合块的大小和类型,对于大多数组织,18-24h较为理想,细胞固定时间较短,一般2%的甲醛室温固定20min即可。以细胞样品为例:用4%的多聚甲醛固定爬片15min,PBS浸洗玻片3次,每次3min。
免疫荧光法是将免疫学方法(抗原抗体特异结合)与荧光标记技术结合起来研究特异蛋白抗原在细胞内分布的方法。由于荧光素所发的荧光可在荧光显微镜下检出,从而可对抗原进行细胞定位。用免疫荧光技术显示和检查细胞或组织内抗原或半抗原物质等方法称为免疫荧光细胞(或组织)化学技术。免疫荧光细胞化学是根据抗原抗体反应的原理,先将已知的抗原或抗体标记上荧光素制成荧光标记物,再用这种荧光抗体(或抗原)作为分子探针检查细胞或组织内的相应抗原(或抗体)。在细胞或组织中形成的抗原抗体复合物上含有荧光素,利用荧光显微镜观察标本,荧光素受激发光的照射而发出明亮的荧光(黄绿色或桔红色),可以看见荧光所在的细胞或组织,从而确定抗原或抗体的性质、定位。免疫荧光技术可以通过荧光信号显示和检查细胞或组织内的抗原或半抗原物质。
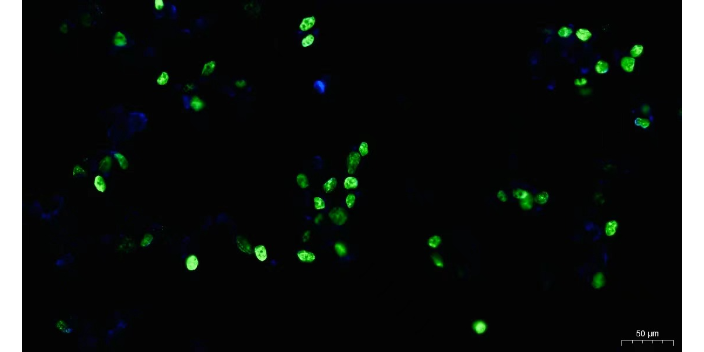
荧光标记二抗的选择普遍;与使用荧光素结合一抗的检测相比,成本较低。间接免疫荧光的缺点:由于需要具有两种不同物种反应性的两种抗体,因此物种交叉反应性问题增加;与直接免疫荧光相比,时间更长(操作步骤更多)。间接免疫荧光的优点:通过增加能够与一抗结合的二抗数量进行信号放大;与直接免疫荧光相比,通过信号放大提高检测灵敏度;荧光标记二抗的选择普遍;与使用荧光素结合一抗的检测相比,成本较低。间接免疫荧光的缺点:由于需要具有两种不同物种反应性的两种抗体,因此物种交叉反应性问题增加;与直接免疫荧光相比,时间更长(操作步骤更多)。免疫荧光技术可以用于研究免疫相关疾病和自身免疫病。P-AKT 1/2/3免疫荧光检查
免疫荧光技术可以用于研究植物病理学和农业生产。P-AKT 1/2/3免疫荧光检查
荧光的产生:一此化学物质能从外界吸收并储存能量(如光能、化学能等)而进入激发态,当其从激发态再回复到基态时,过剩的能量可以电磁辐射的形式放射(即发光)。荧光发射的特点是:可产生荧光的分子或原子在接受能量后即刻引起发光;而一旦停止供能,发光(荧光)现象也随之在瞬间内消失。可以引起发荧光的能量种类很多,由光激发所引起的荧光称为致荧光。由化学应所引起的称为化学荧光,由X线或阴极射线引起的分别称为X线荧光或阴极射线荧光。荧光免疫技术一般应用致荧光物质进行标记。P-AKT 1/2/3免疫荧光检查
上一篇: 苏州细胞实验计划
下一篇: 浙江动物细胞病理实验服务